オゾンの発生方法と分解のしくみ
オゾンには強い酸化力がありますが、最終的に無害な酸素になるため残留毒性がないという利点があり、脱臭、殺菌、洗浄、表面改質等、様々な分野で有効活用されています。
オゾン活用の一例として、下図の低圧水銀ランプを用いたUVオゾン洗浄装置があります。低圧水銀ランプによって生成した紫外線(主波長は185nm、254nm)、オゾン、活性酸素の作用で半導体ウェハーや液晶ディスプレイの表面に付着した有機物を分解してCO2、H2O、O2等の揮発性物質に変えて洗浄します。なお、UVフィルターで185nmをカットしてオゾンを発生させないようにした低圧水銀ランプは、主に殺菌用に使われます。近年は、キセノンエキシマランプの紫外線172nmを用いて効率よく高濃度のオゾンと活性酸素を生成するUVオゾン洗浄装置が注目されています。いずれの方式においても発生したオゾンを全て有効に使い切ることはできないため、残留オゾンの発生は避けられません。
 UV洗浄装置の低圧水銀ランプ
UV洗浄装置の低圧水銀ランプオゾンの発生方法は上記の紫外線照射のほかにも様々あり、代表的なものとして下図に示した無声放電や沿面放電等の放電によるもの、電気分解によるものがあります。
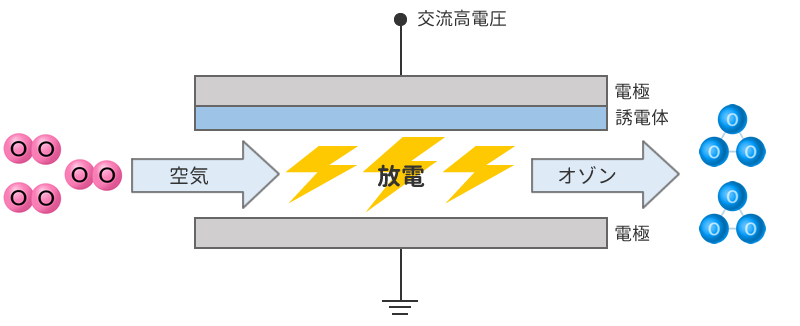 無声放電
無声放電オゾンは濃度が高くなると生体にとって有害であり、大気中で自然分解されて酸素になるまでには一定の時間が必要なため、残留オゾンを速やかに処理する必要が出てきます。当社ではオゾンを分解するマンガン系の金属酸化物触媒をハニカム状に押出成形したフィルターを製造販売しております。日本産業衛生学会による作業環境基準のオゾン許容濃度は0.1ppmであり、一般的にフィルター通過後のオゾン濃度が0.1ppm以下になるように設定します。
| オゾン濃度(ppm) | 人体への影響 |
|---|---|
| 0.01~0.02 | 臭気を感じる場合がある |
| 0.1 | 鼻、喉への刺激を感じる |
| 0.2~0.5 | 視力の低下 |
| 1-2 | 疲労感、頭痛 |
| 5-10 | 脈拍増加、肺水腫をおこす |
| 50~ | 人は1時間で生命が危険な状態になる |
マンガン系の触媒(Mと表記)によるオゾン分解は以下(1)(2)の反応式で説明されます。
触媒Mは反応の前後で変化していないことが分かります。
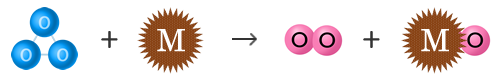
O3 + M → O2 + MO ・・・・・・・・・・(1)
※触媒Mはオゾンと反応してMOになり、酸素が生成される。

O3 + MO → 2O2 + M ・・・・・・・・・・(2)
※MOはオゾンと反応してMに戻り、酸素が生成される。
理想条件において触媒は半永久的に変化しないとされていますが、実際の使用条件では種々の要因により、性能は徐々に低下していきます。大気中には様々なコンタミが存在しており、S(硫黄)やSi(シリコン)のような触媒毒を含む成分が触媒の表面に付着して反応するサイトを塞いでしまうことが考えられます。また、水分も吸着サイトを塞いでしまうため、湿度は低いほどオゾン分解には有利になります。また、結露するような条件では十分に性能を発揮することができません。ただし水分による性能低下は一時的なものであり、熱をかけるなどして水分を飛ばしてしまうことで回復します。
マンガン系の触媒のほかに、活性炭でもオゾンは分解できることが分かっており、以下(3)(4)の反応式が共存していると考えられています。
2O3 + C → CO2 + 2O2 ・・・・・・・・・・(3)
2O3 + C → 3O2 + C ・・・・・・・・・・(4)
(3)式は活性炭の炭素がオゾンと反応して二酸化炭素になるもので活性炭の消耗を伴いますが、(4)式は触媒反応で活性炭自身は変化しません。オゾンの濃度が高いほど(3)の反応が増加して活性炭の消耗が激しくなるため、一般的に活性炭は低濃度のオゾンに、触媒は高濃度のオゾンに適しています。また、反応は発熱反応のため、蓄熱により可燃物である活性炭は燃える可能性があることに注意する必要があります。
当社のオゾン分解触媒フィルターは長い実績と信頼を得ており、オゾンの除去に関してご相談がありましたら、ぜひお気軽にお声がけください。
【参考文献】オゾン分解技術(1990三琇書房)

